Інформація про препарат CR 173487 для спеціалістів
Дослідження препарату
Дослідження препарату CR 173487 проводяться в провідних НДІ України та в медичних установах стосовно переносимості, безпеки, терапевтичної дії, фармакокінетичних і фармакодинамічних характеристик, терапевтичних рівнів дозування, вивчення способів введення, формування протоколів лікування відповідно до поставленого діагноза.
I фаза дослідження, 2007-2009 рр
| Предмети дослідження | Діагнози | Медична установа/керівник досліджень | Лікарняна форма |
Переносимість Гостра токсичність препарата | Пухлини головного мозку:
| Головний онконейрохірург НАМН України, керівник відділу нейроонкології та нейрохірургії дитячого віку Інституту нейрохірургії імені Академіка А.П. Ромоданова НАМН України, член-кореспондент НАМН України, професор, д.м.н., Розуменко Володимир Давидович | Розчин для ін’єкций |
Дослідження дозволили зробити попередні висновки щодо протипухлинної активності препарату:
- клінічне гальмування пухлинного процесу
- процес лікувального апоптозу
- поліпшення якості життя
З 2018 року клінічні дослідження препарата проводяться з низкою агресивних пухлин:
| Внутрішньомозгові пухлини | Пухлини шлунково-кишкового тракту (ШКТ) | Пухлини шлунково-кишкового тракту (ШКТ) | Рак легенів |
Завдяки расширеним дослідженням I-ї фази клінічних іспитів, зафіксовані та затверджені:
- максимально допустимі дози препарату (переносимість)
- дозування ліків, необхідні для лікування того чи іншого виду раку
- спосіб введення препарату (форма застосування)
II фаза клінічних досліджень
II фаза контрольованих рандомізованих клінічних досліждень показала високу ефективність препарату, дозволила скласти попередні протоколи лікування в залежності від діагнозу та інших важливих показників.
III фаза багатоцентрових клінічних дослідждень
Наразі активно проводиться і характерізується позитивними якісними результатами.
Результати досліджень, які вже проведені, вказують на нетоксичність і безпеку препарату. Іншими словами, препарат не чинить токсичної дії на організм людини. Його використання є безпечним для пацієнта, факти прямого токсичного впливу препарату на організм людини до теперішнього часу не зафіксовано.
Реакція на введення препарату часто проявляється незначним підвищенням температури тіла пацієнта в перші 3-5 днів після введення препарату, що свідчить про реакцію імунної системи організму і не вимагає спеціального лікування.
За результатами проведених досліджень представляється можливим зробити попередні висновки про протипухлинну активність препарату: встановлено клінічне гальмування пухлинного процесу, що свідчить на користь лікувального патоморфозу і призводить до поліпшення якості життя (згідно опитувальника ВООЗ).
Звикання до препарату не зафіксовано.
Препарат CR 173487 здатний ввести хворого в тривалу ремісію, вилікувати пацієнта.
Особливості застосування препарата
Застосування препарату дозволяє поліпшити стан здоров’я, практично, всіх онкохворих, так як вже протягом перших двох-трьох тижнів з дня початку лікування в організмі хворого спостерігається руйнування значної частини пухлинних клітин.
Тривалість лікування препаратом
Тривалість лікування препаратом, включаючи процеси реабілітації (виведення і резорбції зруйнованих клітин, відновлення належних функцій організму хворого), залежить від характеру і ступеня тяжкості захворювання. Для хворих, ослаблених прийомом раніше використовуваних високотоксичних ліків і процедур і, які мають кілька зон онкологічного ураження, процес лікування препаратом є поетапним і більш тривалим. Конкретна тривалість курсу лікування препаратом, дози препарату і способи його введення залежать від локалізації, гісто і цитогенезу злоякісної пухлини.
В період лікування препаратом необхідний постійний клінічний контроль здоров’я пацієнта. Важливо виключити неузгоджені до застосування інші лікарські засоби, в тому числі на спиртовій основі. Препарат не можна застосовувати одночасно з променевою і хіміопроменевою терапією, тому що ці методики значно збільшують рівень токсичних речовин в організмі хворого, пригнічують його імунну систему, негативно впливають на можливості організму щодо регенерації тканин, нівелюють дію препарату. Інтервал між прийомом препарату CR 173487 та іншими методами впливу на пухлину (хіміотерапія, променева терапія) повинен складати не менше 7 днів.
Дієтична добавка ТІОСАН® – нові можливості для паціентів
В 2016 році фармацевтична компанія КРАУН ФАРМА зареєструвала новий продукт – дієтичну добавку ТІОСАН, котра призначена для перорального вживання і використовується в якості засобу для оптимізації лікування злоякісних новоутворень (висновок державної санітарно-епідеміологічної експертизи №602-123-29-2/2525 від 05.12.2016 р., ТУ У 10.8-40893378-001:2016; протокол досліджень № 3/8-А-3811-17-64752Е від 31.07.2017 р.).
С грудня 2017 року і до теперішнього часу в Інституті нейрохирургії ім. академіка А. П. Ромоданова НАМН України проводяться клінічні дослідження стосовно використання дієтичної добавки ТІОСАН у паціентів з установленим діагнозом гліобластома і/або анапластична гліома (2 протоколи клінічних досліджень).
| Предмет дослідження | Діагноз | Медична установа/керівник досліджень | Лікарняна форма |
| Переносимість та ефективність |
| Головний онконейрохірург НАМН України, керівник відділу нейроонкології та нейрохірургії дитячого віку Інституту нейрохірургії імені Академіка А.П. Ромоданова НАМН України, член-кореспондент НАМН України, професор, д.м.н., Розуменко Володимир Давидович | Розчин для перорального використання |
Попередні результати свідчать про позитивний вплив цього продукту на хід лікування внутрішньомозкових онкозахворювань III і IV ступеня злоякісності.
ТІОСАН покращує якість життя пацієнтів, не викликає побічної симптоматики, прояви токсичності не спостерігалися.
Реакція на продукт часто проявляється незначним підвищенням температури тіла пацієнта в перші 3 — 5 днів після прийому, що свідчить про реакцію імунної системи організму і не вимагає спеціального лікування.
Звикання до продукту на даний момент не зафіксовано.
ТИОСАН нешкідливий при застосуванні.
ТІОСАН може застосовуватися при лікуванні різних онкологічних процесів.
Накопичуються дані стосовно його ефективності.
МЕХАНІЗМ ДІЇ ПРОТИРАКОВОГО ПРЕПАРАТУ CR 173487
Завдяки компонентам, які входять до складу біологічно-активної субстанції, препарат має ряд структурних особливостей, які забезпечують унікальність его біофізичних і біохімічних характеристик.
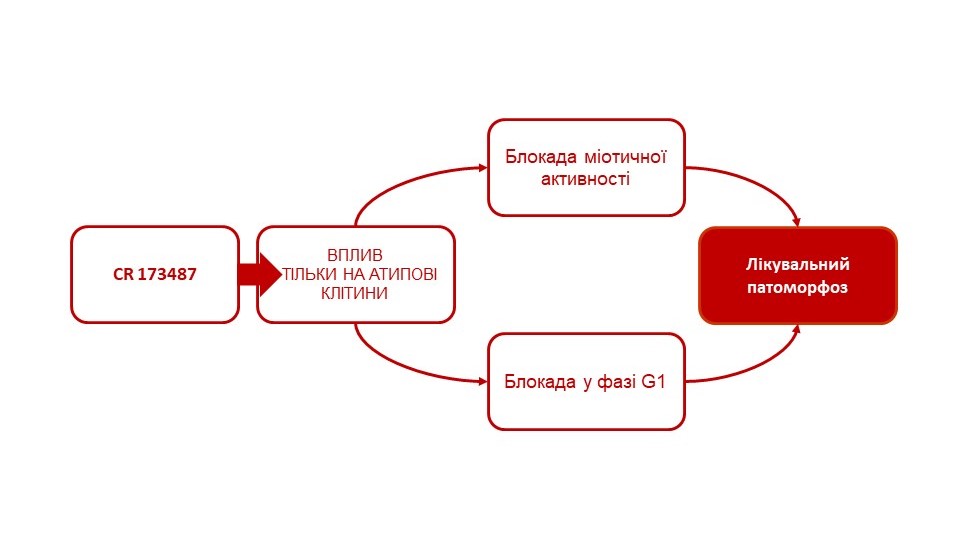
Дослідження in vitro та in vivo підтвердили, що препарат діє виключно на атипові клітини у процесі їхнього мітозу та в ході підготовки клітин до поділу. Іншими словами, CR 173487 проявляє свою цитотоксичну здатність на 80% в період метафази-телофази і на 20% — в період раннього дозрівання атипової клітини у ранній G1 фазі.
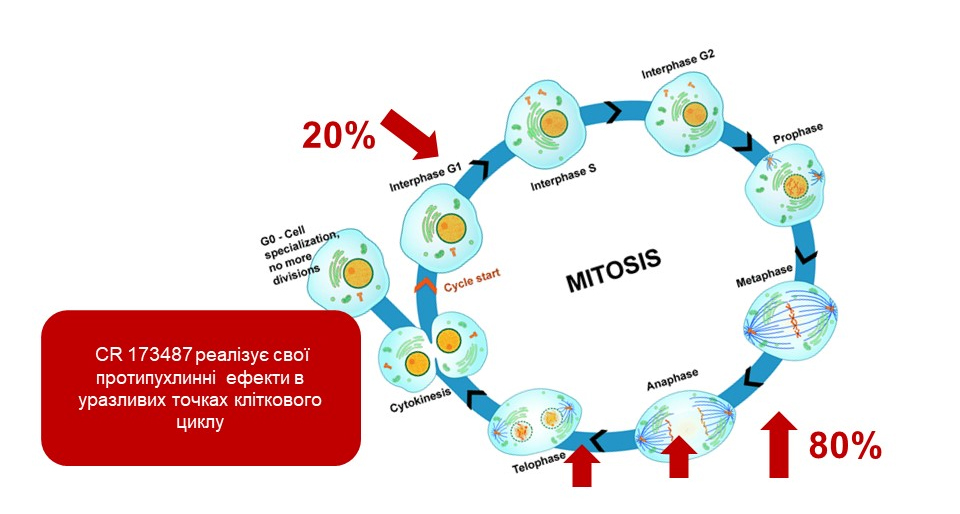
Застосування препарату доцільно як на ранніх стадіях раку, так і на більш пізніх, коли підключається процес метастазування.
Протипухлинна дія препарату проявляється в період розмноження атипових клітин переважно за допомогою блокування мітозу. В результаті цього процесу нежиттєздатні клітини піддаються лікувальному патоморфозу і утилізуються макрофагами.
Так досягається контроль над захворюванням навіть на пізніх стадіях.